MECANISMO DE EVASIÓN DE LA RI
Tanto el SARS-CoV como el MERS-CoV tienen mecanismos que les permiten pasar desapercibidos por la respuesta inmunitaria del huésped y evitar que se desencadene el “estado antiviral”. Estos hCoV virulentos codifican proteínas estructurales y no estructurales o “nsps”, tales como nsp1 o nsp3.
Tanto nsp1, como nsp3 son capaces de antagonizar la vía de señalización de IFN. En el caso de nsp3, no se conoce bien el mecanismo, mientras que nsp1 es capaz de anular la fosforilación de STAT-1, un factor de transcripción que participa en la señalización mediada por IFN-I e induce un “estado antiviral” cuando entra al núcleo de las células huésped infectadas. Si bien, también se han visto implicadas proteínas estructurales como la nucleocápside o proteína N y la membrana (M).
Por lo tanto, las respuestas antagónicas generadas sobre la vía del IFN-I por parte de las proteínas estructurales y no estructurales, no solo evitan una respuesta innata eficiente, sino que promueven una rápida expansión del virus y una gran tormenta de citoquinas y quimioquinas proinflamatorias que conducen a un reclutamiento desmesurado de neutrófilos y monocitos al lugar de la infección.
Cabe destacar el papel de la proteína E estructural, presente en estos hCoV más patógenos. Esta proteína pentamérica de membrana posee actividad de canal iónico y permite la activación del inflasoma en las células huésped. Este inflasoma es el responsable de la producción de citoquinas proinflamatorias como TNF-α, IL-1β e IL-6. La liberación de estas citoquinas promueve una respuesta inflamatoria no controlada en el pulmón del huésped, que conduce a una hiposemia grave, edema y ocasionalmente la muerte.
Para comprobar la función de la proteína E, se diseñaron dos SARS-CoV recombinantes a los cuales se les indujo una sola mutación de un aminoácido (N15A y V25F). Estos virus recombinantes se introdujeron a ratones y se comprobó que tenían su proteína E inactivada, ya que no se produjo la activación del inflasoma, con lo cual no se liberaron las citoquinas proinflamatorias y, por tanto, no se desencadenó la respuesta inflamatoria descontrolada o hiperinflamación.
INMUNOPATOLOGÍA
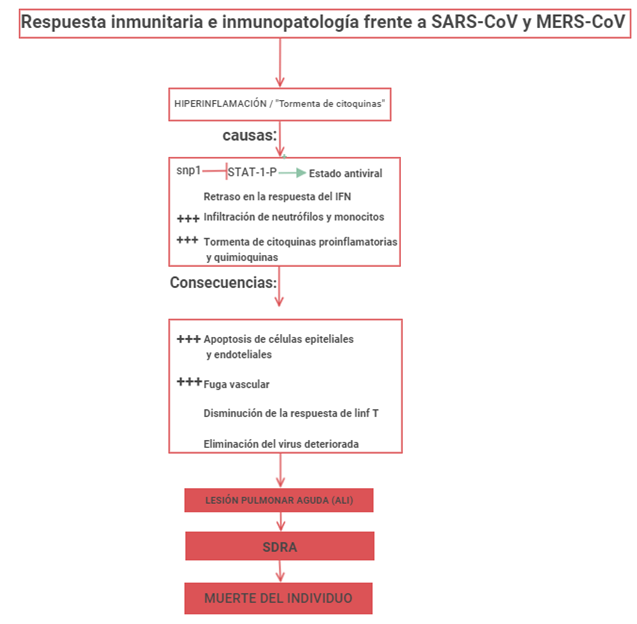
Como resultado de la “tormenta de citoquinas” generada por estas cepas virulentas y la evasión de la respuesta inmune innata por medio de la inhibición de la vía del IFN-I, se produce una rápida replicación de los virus y la apoptosis de células endoteliales y epiteliales debido a la hiperinflamación generada. Esto provoca un derrame vascular, que puede conducir a un edema alveolar y seguidamente provocar una hipoxemia severa.
Además, esta respuesta inflamatoria descontrolada y generada es capaz de disminuir la respuesta de linfocitos T, ya que se induce la apoptosis de los mismos mediante TNF-α y esto es de vital importancia, ya que la respuesta de linfocitos T-CD8+ es muy importante en la RI adaptativa frente a la mayoría de virus.
También, la excesiva infiltración de neutrófilos y células de la serie monocito-macrófago y la liberación de citoquinas proinflamatorias como IL-1β e IL-6 entre otras conducen al SDRA o síndrome de dificultad respiratoria aguda. Este es uno de los cuadros más graves, ya que el tejido pulmonar puede fibrosarse como consecuencia de la inflamación excesiva y conducir a la muerte del individuo.
En definitiva, el control de la RI innata frente al SARS-CoV y MERS-CoV es indispensable, ya que, de no producirse una respuesta de INF-I rápida y eficaz, el virus se propaga mucho más rápido, generando a su vez una «tormenta de citoquinas» proinflamatorias que provocan patologías muy graves en los huésped infectados, llevando incluso a la muerte en el peor de los casos.